CAR改変細胞の特性解析用ソリューション
キメラ抗原受容体 (CAR) ベースの細胞療法は、ヒトのがんや自己免疫疾患の治療に革新をもたらしています。この画期的な治療モダリティは、改良され続けて、より利用しやすくなりつつあります。それに伴い、優れた試薬が登場し、CAR発現細胞の検出や特定、完全な特性解析を行う能力は向上しています。CSTは、画期的な製品のラインナップをますます拡大し、この分野の研究者の研究をサポートしています。
CAR改変細胞をより簡単に、より迅速に特性解析可能
CAR改変細胞を確実に特定できる、感度の高い特異的な研究試薬を用意することは、CAR改変細胞の開発と特性解析を行う科学者が直面する重要な課題の1つです。免疫アッセイプラットフォームで研究を行う際の、CAR改変細胞の特定用の抗イディオタイプ抗体を独自に開発するプロセスは、長い時間とリソースを必要とします。
CAR遺伝子改変細胞の特性解析ワークフロー用のソリューション
CAR改変細胞を特性解析するための複雑なプロセスには、多くのステップが含まれます。CSTは、各プロセスの特に重要なステップに役立つ、CAR改変細胞の特性解析用の一連の研究ツールを提供しています。
CSTの科学者は、特性解析アッセイを効率化するために、scFVベースのCARに一般的に用いられるペプチドリンカー配列に対するリコンビナントモノクローナル抗体を開発しました。これらの一般的なリンカー配列を標的化することにより、試験に用いるCAR変異体ごとに抗イディオタイプ抗体を作製する必要がなくなり、実験にかかる時間や労力、コストを大幅に削減できます。G4SリンカーまたはWhitlow/218リンカーに対する、特異性の高い弊社のCARリンカー抗体は、scFvの特異性にかかわらずscFvベースのCARの発現を検出できます。
CARの検出
- フローサイトメトリー用G4Sリンカー抗体
- scFv抗原の特異性にかかわらず、細胞表面に発現するG4Sリンカーを含むscFvベースのCARを検出可能
- 複数のパラメーターを検出するフローサイトメトリーパネルにおいて高い性能を発揮
- フローサイトメトリー用Whitlow/218リンカー抗体
- scFv抗原特異性にかかわらず、細胞表面に発現するWhitlow/218を含むscFvベースのCARを検出可能
- 複数のパラメーターを検出するフローサイトメトリーパネルにおいて高い性能を発揮
- CARリンカー標識抗体F (ab') 2フラグメント
- Protein L標識抗体
- CARリンカーELISAキット
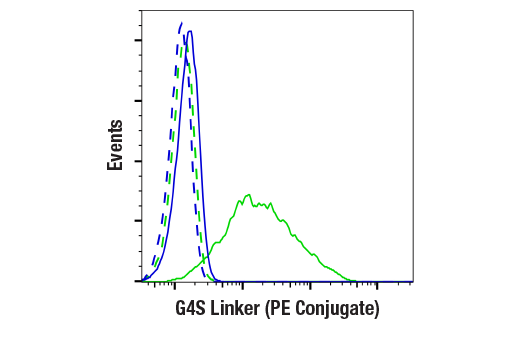
Jurkat細胞の生細胞 (青) またはG4Sリンカーを含むscFvベースの抗CD20 CARを安定して発現するように改変したJurkat細胞 (緑) を、G4S Linker (E7O2V) Rabbit mAb (PE Conjugate) (実線) または同じ濃度のRabbit (DA1E) mAB IgG XP® Isotype Control PE Conjugate #5742 (破線) を用いてフローサイトメトリーで解析しました。細胞株は、Lohmueller研究室 (ピッツバーグ大学) からご提供いただきました。
コントロール
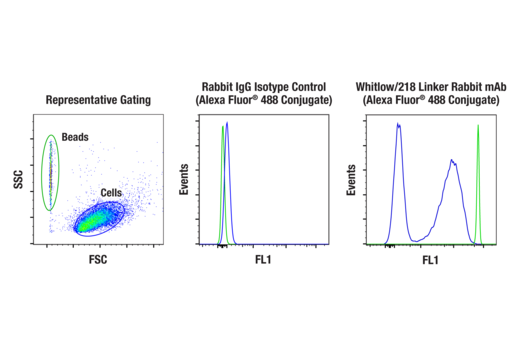
野生型Jurkat細胞、およびWhitlow/218リンカーを含むscFvベースの抗CD19 CARを発現するように改変したJurkat細胞の混合サンプルに、Whitlow/218 Linker Posibeads™を追加しました。次に、各細胞とPosibeadコントロールを、Rabbit (DA1E) mAb IgG XP® Isotype Control (Alexa Fluor® 488 Conjugate) #2975 (中央) またはWhitlow/218 Linker (E3U7Q) Rabbit mAb (Alexa Fluor® 488 Conjugate) #55809 (右) を用いて免疫染色してフローサイトメトリーで解析しました。各細胞とビーズを、図に示すように前方散乱光 (FSC) と側方散乱光 (SSC) を用いて区別しています (左)。また、2種類の免疫染色条件下おける細胞 (青) とPosibeadsコントロール (緑) の蛍光データ (FL1) を示しています (中央、右)。CAR細胞株は、Lohmueller研究室 (ピッツバーグ大学) からご提供いただきました。
標的抗原検出
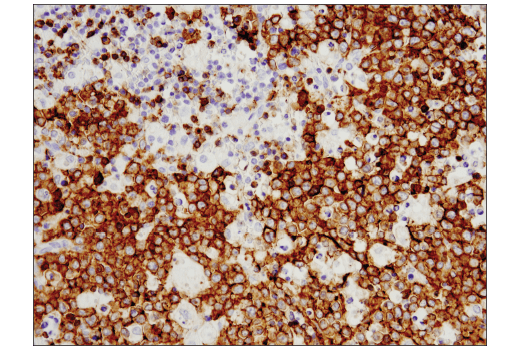
パラフィン包埋ヒトリンパ腫組織を、CD19 (Intracellular Domain) (D4V4B) XP® Rabbit mAb #90176を用いて免疫組織化学染色で解析しました。
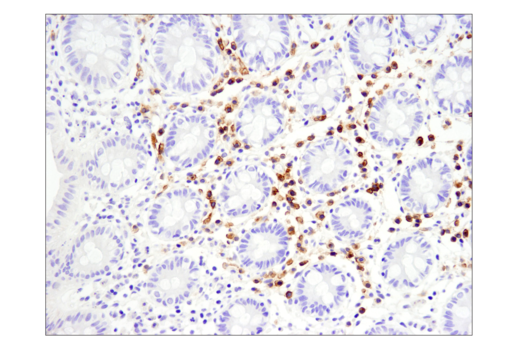
パラフィン包埋ヒト正常結腸組織を、TNFRSF17/BCMA (E6D7B) Rabbit mAb #88183を用いて免疫組織化学染色で解析しました。
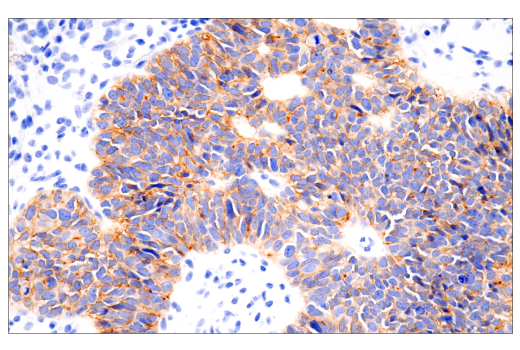
パラフィン包埋ヒト卵巣漿液性乳頭状腺がん組織を Claudin-6 (E7U2O) XP® Rabbit mAb #18932を用いて免疫組織化学染色し、Leica BOND Rxで解析しました。
T細胞活性化
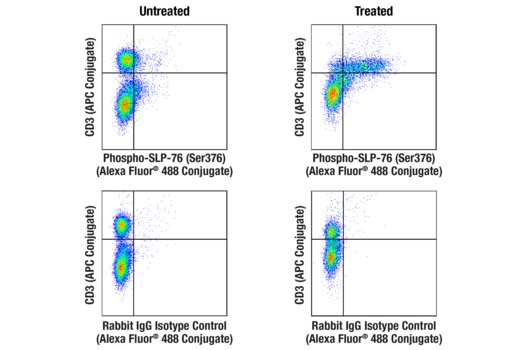
マウス脾細胞を、未処理 (左) またはRapid-Act T-Cell Activation Kit #86772 (マウス、抗CD3/CD28) で処理し (15分間、右)、Phospho-SLP-76 (Ser376) (E3G9U) XP® Rabbit mAb (Alexa Fluor® 488 Conjugate) #47876 (上) または同濃度のRabbit (DA1E) mAb IgG XP® Isotype Control (Alexa Fluor® 488 Conjugate) #2975 (下)、および共染色用のCD3 (17A2) Rat mAb (APC Conjugate) #24265を用いてフローサイトメトリーで解析しました。
細胞増殖
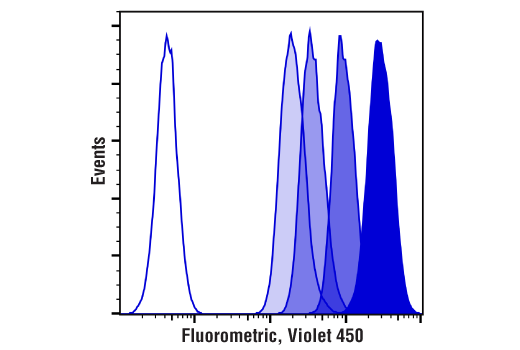
Jurkat細胞 (生細胞) の細胞分裂を4日間 (d0-d3) 追跡しました。Day 0にCell Proliferation Tracer Kit (Fluorometric, Violet 450) #48444 を用いて細胞を標識し、各日にフローサイトメトリーで解析しました。徐々に色が薄くなっている各ピークが、それぞれ1回の細胞分裂を示しています。未染色の細胞を白抜きのピークで示しています。
細胞毒性
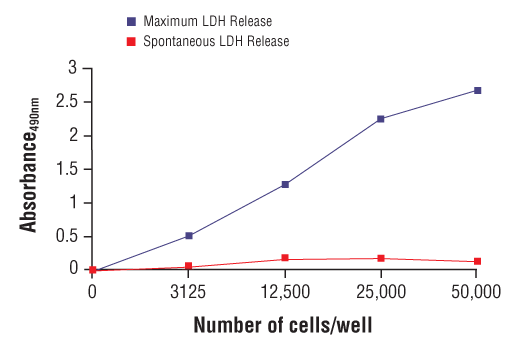
10% FBSを含む培地を用い、HeLa細胞を異なる密度で96ウェルプレートに播種しました。一晩培養した後、無血清培地に交換し、Assay Buffer (LDHを自然放出する) または10% Triton X-100 solution (LDHを最大限に放出する) で処理しました。その後、培地を回収して新しい96ウェルプレートに移しました。培地中に放出されたLDHの量を、LDH Cytotoxicity Assay Kit #37291のプロトコールを用いて測定しました。
フローサイトメトリーによる免疫表現型解析
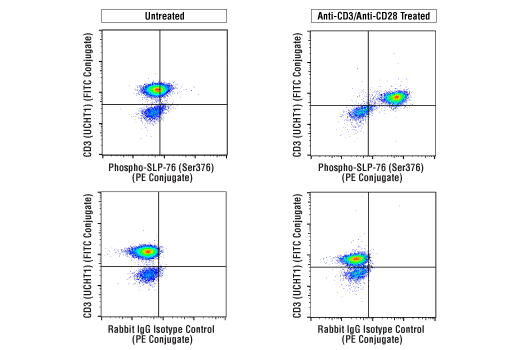
未処理のヒト末梢血単核細胞細胞 (左) またはクロスリンクした抗CD3および抗CD28で処理 (それぞれ10 µg/ml、15分間) したヒト末梢血単核細胞細胞 (右) を、Phospho-SLP-76 (Ser376) (E3G9U) XP® Rabbit mAb (PE Conjugate) #76143 (上)、もしくは同濃度のRabbit (DA1E) mAb IgG XP® Isotype Control (PE Conjugate) #5742 (下)、および共染色としてCD3 (UCHT1) Mouse mAb (FITC Conjugate) #86774を用いてフローサイトメトリーで解析しました。
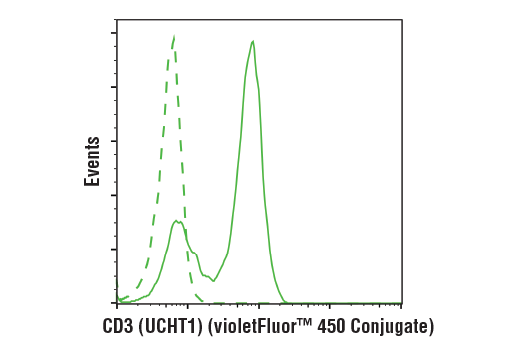
CD3 (UCHT1) Mouse mAb (violetFluor 450 Conjugate) #61347 (実線) または同濃度のMouse (MOPC-21) mAb IgG1 Isotype Control (violetFluor 450 Conjugate) #40282 (破線) で染色したヒト末梢血単核細胞 (生細胞) を、フローサイトメトリーで比較解析しました。
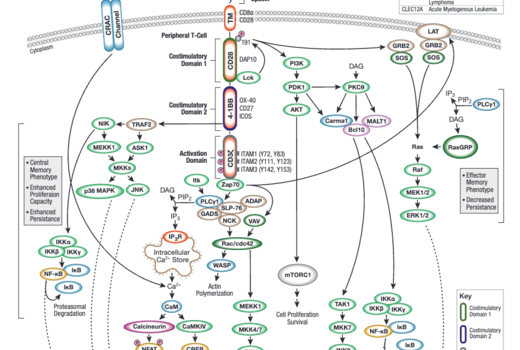
CAR-T細胞活性化における下流シグナル伝達の指標
CAR分子の細胞表面発現の測定
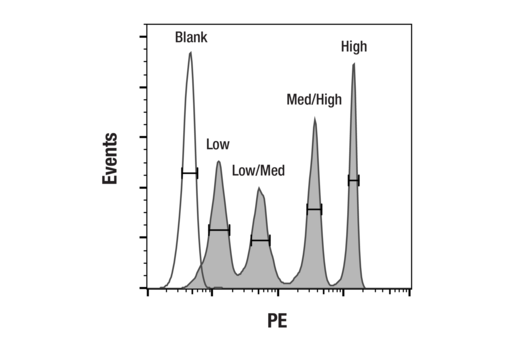
PE標識ビーズと未標識ビーズの4つの蛍光強度の代表的なフローサイトメトリーヒストグラムを重ね合わせたグラフ
CAR導入効率のモニタリング
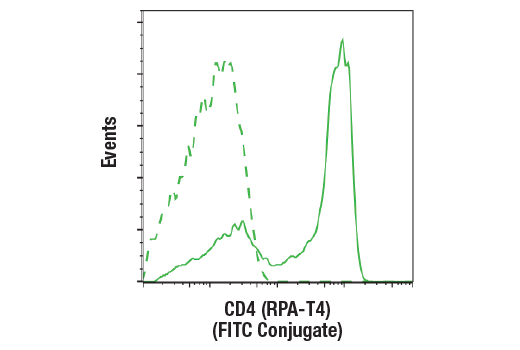
ヒト末梢血単核細胞 (生細胞) をCD4 (RPA-T4) Mouse mAb (FITC Conjugate) (実線) または同濃度のMouse (MOPC-21) mAb IgG1 Isotype Control (FITC Conjugate) #97146 (破線) で染色し、フローサイトメトリーで解析しました。
CAR陽性細胞のビーズベースのソーティング
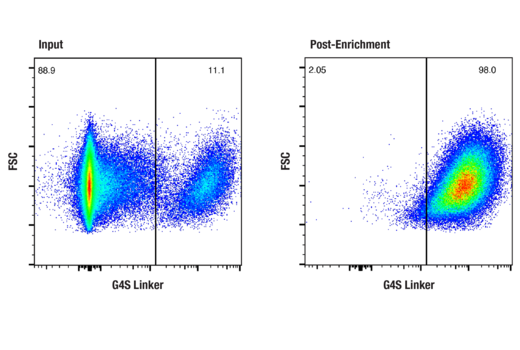
インプット (左) および濃縮後 (右) の生細胞を、ビオチン標識G4S Linker (E7O2V) Rabbit mAbを用いてフローサイトメトリーで解析しました。インプットは、G4Sリンカーを含むscFvベースの抗CD20 (Leu16) CARが遺伝子導入されていない細胞とされている細胞が混在している、CD4陽性/CD8陽性ヒトT細胞で構成されます。濃縮後のサンプルは、細胞表面にCARを発現する細胞のほぼ純粋な集団であることが分かります。ビオチン標識抗体を検出する二次抗体に、Anti-rabbit IgG (H+L), F(ab')2 Fragment (Alexa Fluor® 647 Conjugate) #4414を使用しました。
CAR陽性細胞のFACSベースのソーテイング
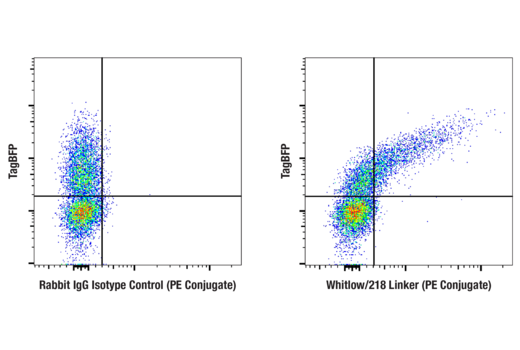
ヒトPBMCから単離し、Whitlow/218リンカーを含むscFvベースの抗CD19 CARを発現するように改変した汎CD3陽性T細胞を、Whitlow/218 Linker (E3U7Q) Rabbit mAb (PE Conjugate) #62405 (右) または同じ濃度のRabbit (DA1E) mAb IgG XP® Isotype Control (PE Conjugate) #5742 (左) を用いてライブセルフローサイトメトリーで解析しました。TagBFP (Tag Blue fluorescent protein) をCARと共発現させています。データは、Lohmueller研究室 (ピッツバーグ大学) のMicahel Kvrjak博士からご提供いただきました。
トランスレーショナルリサーチ用のツール
固形がんの治療にCARを用いる際の最も重要な課題は、これらの細胞が、がん微小環境に侵入できる能力を持っているかどうかです。従来の評価方法には、大きな欠点がいくつかありました。しかし、幸いなことに、現在では市販の抗体を用いて固形がん内におけるCARタンパク質の発現を直接調べることが可能になりました。
組織内のCAR発現を研究する
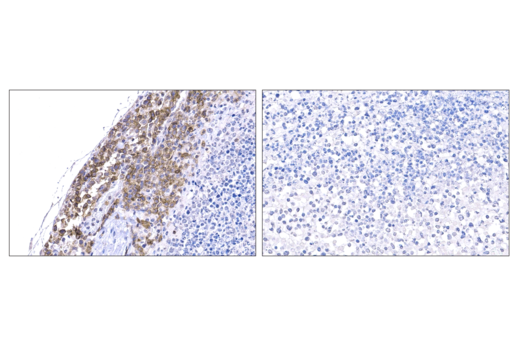
初代ヒト抗CD19 CAR-T細胞 (左) またはPBSコントロール (右) を血中に戻したNSGマウス脾臓におけるRaji B細胞リンパ腫異種移植片組織を、Whitlow/218 Linker (F2G3S) Rabbit mAb #47414を用いて免疫組織化学染色で解析しました。
がん微小環境の調査
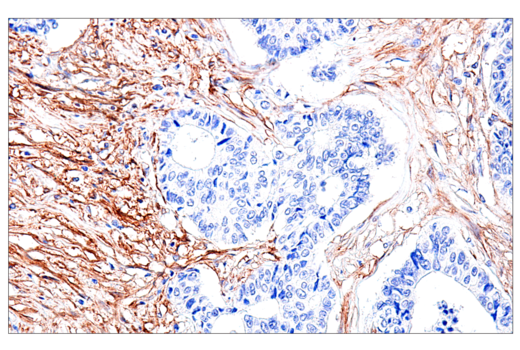
パラフィン包埋ヒト結腸がんを、FAP (F1A4G) Rabbit mAb #52818を用いて免疫組織化学染色で解析しました。
CAR改変細胞の特性解析用リソース
CAR細胞の特性解析に着目したウェビナーや科学ポスター、アプリケーションノート、その他のリソースなどを含む、ますます拡大する弊社のライブラリーを探索してください。
ウェビナーとビデオ
CARリンカー抗体で、CARパネル全体の発現を調査する方法を紹介
CAR-T細胞シグナル伝達と活性化を評価するための解析ツール (45:23)
Bio-Techne社の解析装置とCSTの抗CARリンカー抗体を用いて、CD19 CAR-T細胞作製のワークフローを効率化する方法を紹介
汎用性のある画期的な抗体を用いたCARの発現の検出 (2:04)
CSTが提供する画期的な抗リンカーモノクローナル抗体を用いて、新たなキメラ抗原受容体 (CAR) 分子の開発のたびに固有の検出試薬を開発することなく、フローサイトメトリーパネルの検出を加速する方法を紹介
最新の発表ポスター
- Generation and Validation of Anti-Linker Monoclonal Antibodies for the Surface Detection of scFv-based CARs (ビデオ、5:25)
- Generation and validation of anti-linker monoclonal antibodies for the detection of surface expressed scFv-based CARs (PDF、1MB)
- A novel monoclonal antibody for the detection, enrichment and activation of cells expressing scFv-based chimeric antigen receptors (PDF、2.2MB)
よくある質問
G4S Linker (E7O2V) Rabbit mAbは、G4Sを1つだけ含むscFvベースのCARを検出できますか? | いいえ。E7O2Vが、scFvベースのCARに適切に結合するには、2つ以上のG4S配列が必要です。 |
G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbのKd (解離定数) は既知ですか? | はい。G4S Linker (E7O2V) Rabbit mAbのKdは約1 - 2 nM、Whitlow/218 Linker (E3U7Q) Rabbit mAbのKdは約2.5 nMです。 |
G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbが、抗原特異性の異なるscFvに結合するかを試験していますか? | はい。G4S Linker (E7O2V) Rabbit mAbは4種類の異なるscFvに、Whitlow/218リンカーも4種類の異なるscFvに結合することを確認しています。 |
G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbが、FFPE組織内のCAR改変細胞を検出できるかを試験していますか? | はい。残念ながら、G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbは、どちらもFFPE組織内のCAR改変細胞の検出に適していません。しかし、弊社は、FFPEのIHCでの使用が承認されたWhitlow/218 Linker (F2G3S) Rabbit mAbを提供しています。 |
G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbが、細胞抽出物中のCARをウェスタンブロッティングで検出できるかを試験していますか? | はい。残念ながら、G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbはどちらも、従来の免疫ブロット法を用いた細胞抽出物中のCARタンパク質の検出に適していません。しかし、Whitlow/218 Linker (E3U7Q) Rabbit mAbは、Simple WesternプラットフォームのJess装置での使用が承認されています。また、Whitlow/218 Linker (F2G3S) Rabbit mAbは、ウェスタンブロッティングでの使用が承認されています。 |
G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbが、固定した細胞、または固定および透過化した細胞のCARをフローサイトメトリーで検出できるかを試験していますか? | はい。G4S Linker (E7O2V) Rabbit mAbとWhitlow/218 Linker (E3U7Q) Rabbit mAbはいずれも、生細胞を用いたフローサイトメトリーアッセイで細胞表面に発現するCARを検出します。染色の前に固定または固定/透過化した細胞の使用は推奨していません。 |
FDA承認済みのCARコンストラクトに使用されているペプチドリンカーは何かを教えていただけますか? | はい。Yescarta、Tecartus、Breyanzi、AbecmaのすべてにWhitlowリンカーが含まれます。Kymriahには3X-G4Sリンカー、Carvyktiには1X-G4Sリンカーが含まれます。 |
Magnetic CAR T cell purification using an anti-G4S linker antibody.
市販されているCSTのG4S Linker (E7O2V) Rabbit mAb (PE Conjugate) #38907により、CAR-T細胞の新しい精製方法が開発されました。著者らは、細胞生存率に影響を与えることなく、ワンステップでCAR-T細胞が高度に濃縮できたことを報告しており、CST抗体の特異性と性能が、この精製方法の成功を導いたと考えられます。
Harrer DC, Li SS, Kaljanac M, et al. Magnetic CAR T cell purification using an anti-G4S linker antibody. J Immunol Methods. 2024;528:113667. doi:10.1016/j.jim.2024.113667
Linker-specific monoclonal antibodies present a simple and reliable detection method for scFv-based CAR NK cells
本研究は、CSTが提供するWhitlow/218リンカーおよびG4Sリンカー特異的モノクローナル抗体が、scFvベースのCAR-NK細胞の検出および解析にいかに有用であるかを示しています。これらの感度と特異性の高い抗体は、in vitroでの培養、全血サンプルや腫瘍スフェロイドでの検出などの様々な実験条件下における、フローサイトメトリーを用いたCAR-NK細胞の正確な特定に使用されました。さらに、本研究は、機能アッセイやCAR-NK細胞のポジティブセレクションにおける抗体の役割に着目しており、CAR-NK細胞の研究と臨床応用を進める上で、弊社の汎用性の高いCARリンカー抗体がいかに有用であるかを示しています。
Schindler K, Ruppel KE, Müller C, Koehl U, Fricke S, Schmiedel D. Linker-specific monoclonal antibodies present a simple and reliable detection method for scFv-based CAR NK cells. Mol Ther Methods Clin Dev. 2024;32(3):101328. doi:10.1016/j.omtm.2024.101328 (2024年8月22日)
Synthetic immune checkpoint engagers protect HLA-deficient iPSCs and derivatives from innate immune cell cytotoxicity
本研究は、HLA欠損-人工多能性幹細胞 (iPSC) とその誘導体の免疫回避を強化するための、合成免疫チェックポイントエンゲージャーの改変について報告しています。この研究の鍵となる実験では、エンゲージャーの細胞表面の発現と潜在的な調節効果の評価に、CSTのビオチン標識G4S Linker F(ab')2 Fragmentが使用されています。この抗体フラグメントにより、エンゲージャーの発現レベルと相互作用の詳細なフローサイトメトリー解析が可能となっており、免疫回避戦略の最適化におけるその有用性が示されています。
Gravina A, Tediashvili G, Zheng Y, et al. Synthetic immune checkpoint engagers protect HLA-deficient iPSCs and derivatives from innate immune cell cytotoxicity. Cell Stem Cell. 2023;30(11):1538-1548.e4. doi:10.1016/j.stem.2023.10.003
CSTが提供するCAR改変細胞の特性解析ソリューションが使用された、その他の論文の要約を読む
CARタンパク質検出ツール | 機能 |
|---|---|
G4Sモノクローナル抗体 |
|
Whitlow/218モノクローナル抗体 |
|
Protein L |
|
エピトープタグ抗体 (Myc、FLAG、HA) |
|
CAR発現のサロゲートマーカー (GFP、TagBFP、LNGFR) |
|
抗イディオタイプモノクローナル抗体 |
|
組換えCAR標的抗原 |
|
- Mohanty R, Chowdhury CR, Arega S, Sen P, Ganguly P, Ganguly N. CAR T cell therapy: A new era for cancer treatment (Review). Oncol Rep. 2019;42(6):2183-2195. doi:10.3892/or.2019.7335
- Li JH, Chen YY. A Fresh Approach to Targeting Aging Cells: CAR-T Cells Enhance Senolytic Specificity. Cell Stem Cell. 2020;27(2):192-194. doi:10.1016/j.stem.2020.07.010
- Tenspolde M, Zimmermann K, Weber LC, et al. Regulatory T cells engineered with a novel insulin-specific chimeric antigen receptor as a candidate immunotherapy for type 1 diabetes. J Autoimmun. 2019;103:102289. doi:10.1016/j.jaut.2019.05.017
- Wang D, Starr R, Alizadeh D, Yang X, Forman SJ, Brown CE. In Vitro Tumor Cell Rechallenge For Predictive Evaluation of Chimeric Antigen Receptor T Cell Antitumor Function. J Vis Exp. 2019;(144):10.3791/59275. doi:10.3791/59275 (2019年2月27日)