トランスレーショナルリサーチにおけるPTMScan® Discovery (事例研究)
基礎研究から臨床へ
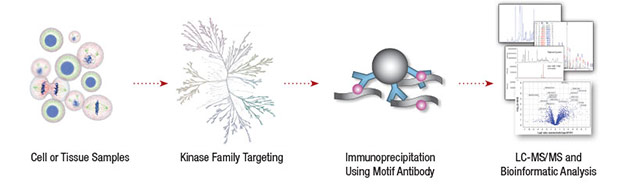
CSTは、非小細胞肺がん (NSCLC) におけるチロシンキナーゼ活性の大規模解析を行い、新規の疾患誘発因子を特定しました (1)。リン酸化チロシン抗体を用いて、NSCLC細胞株41種およびNSCLC腫瘍150症例からリン酸化ペプチドを濃縮し、LC-MS/MS解析を行いました。その結果、2700種以上のタンパク質上から、4551箇所のリン酸化チロシン残基が同定されました。この解析でトップヒットした上位10に、チロシンキナーゼALK (Anaplastic Lymphoma Kinase) が含まれていました。
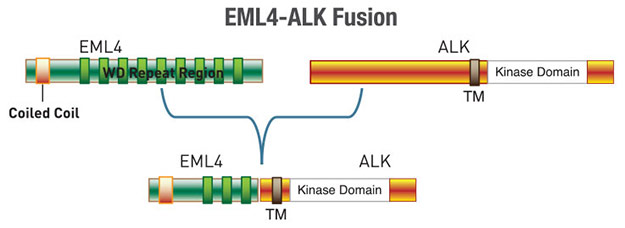
さらに研究を進め、NSCLC細胞株および腫瘍症例の一部では、ALKのC末端とEML4 (Echinoderm Microtubule-associated protein-like 4) のN末端が融合していることが分かりました。3-7%のNSCLC患者の腫瘍組織でこの融合タンパク質が発現していることが明らかにされ、この融合タンパク質が高い発がん性をもつことが示唆されています (1-4)。EML4-ALK融合タンパク質を発現しているがん細胞は、低分子ALK阻害薬クリゾチニブが奏効するため、2011年にクリゾチニブのALK陽性NSCLCへの適用がFDAに認可されました (2)。
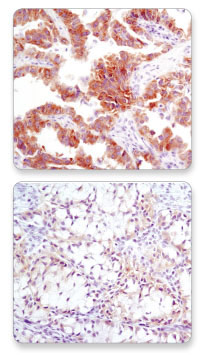
CSTは高い特異性と感度を備えた抗体、ALK (D5F3®) XP® Rabbit mAb #3633を開発しました。この抗体は全長ALKとEML4-ALK融合タンパク質を検出します。このCSTがライセンス化したALK抗体 (クローンD5F3) を用いた、免疫組織化学染色 (IHC) によるコンパニオン診断が、FDAに認可されています (3)。この診断は、医師がNSCLC患者にクリゾチニブの投与を判断する際に役立っています。
参考文献
- Rikova K, Guo A, Zeng Q, Possemato A, Yu J, Haack H, Nardone J, Lee K, Reeves C, Li Y, Hu Y, Tan Z, Stokes M, Sullivan L, Mitchell J, Wetzel R, Macneill J, Ren JM, Yuan J, Bakalarski CE, Villen J, Kornhauser JM, Smith B, Li D, Zhou X, Gygi SP, Gu TL, Polakiewicz RD, Rush J, Comb MJ (2007) Global survey of phosphotyrosine signaling identifies oncogenic kinases in lung cancer. Cell 131(6), 1190–203.
- FDA approves Xalkori with companion diagnostic for a type of late-stage lung cancer
- Ventana receives FDA approval for the first fully automated IHC companion diagnostic to identify lung cancer patients eligible for XALKORI® (crizotinib)