View in English?
View in English?
アポトーシス、マイトファジー、ネクロプトーシス、オートファジーなどの細胞死パスウェイの変異は、神経細胞死や神経変性疾患の進行に寄与します。アポトーシス促進性および抑制性シグナル伝達の異常、ミトコンドリアの機能不全、オートファジーや小胞体ストレス応答の誤制御、ストレスや炎症によるネクロソームの活性化は、神経細胞死や疾患を引き起こすメカニズムのごく一部です。これらのパスウェイの多くは非神経細胞での理解が進んでいますが、ニューロンにおけるその活性化メカニズムや調節不全については謎のまま独自の課題が残されています。
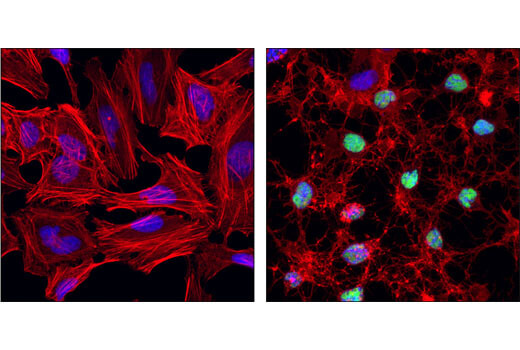
PARPは通常、酸化ストレスに応答したDNA修復パスウェイの重要な制御因子として機能します。Caspase-3によってAsp214とGly215の間が切断されると、切断されたN末端側の断片は、DNA修復酵素を阻害してニューロンをアポトーシスに向け、アポトーシス細胞の特性を示すようになります。
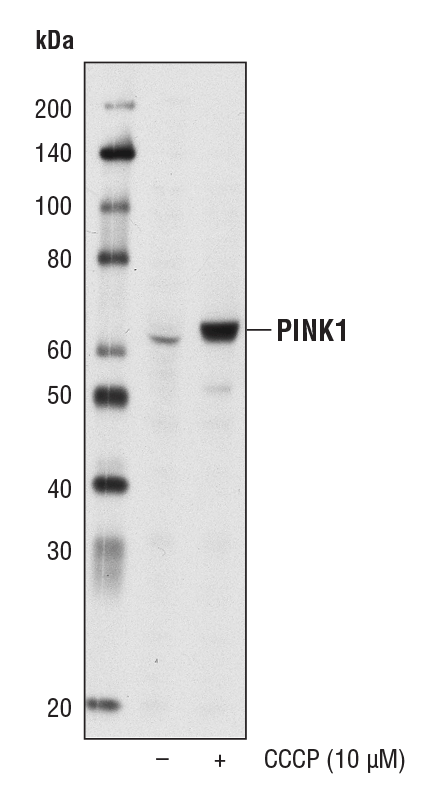
PINK1 (PTEN-induced kinase 1) は、ミトコンドリアのセリン/スレオニンプロテインキナーゼで、ストレス誘導性のミトコンドリア機能障害から細胞を保護します。これはひどく損傷したミトコンドリアの外膜に蓄積し、PARKINをリクルートしてオートファジーによる分解を誘導します。PINK1の変異は、常染色体劣性早発性パーキンソン病と関連しています。
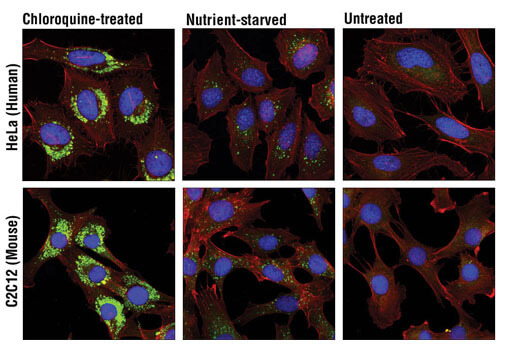
Sequestosome 1 (SQSTM1、p62) はオートファゴソームのカーゴタンパク質で、タンパク質凝集体に結合して選択的オートファジーによる分解に導きます。SQSTM1/p62の変異は、それぞれパーキンソン病、ハンチントン病、アルツハイマー病の進行を促進させる、α-Synuclein、Huntingtin、Tauタンパク質およびβ-Amyloidの細胞内凝集体を増加させます。
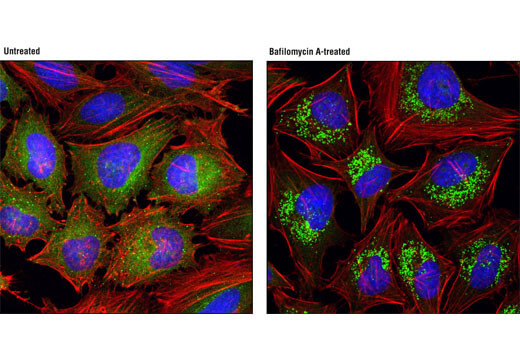
LC3A/Bはオートファゴソームの形成と成熟に重要な役割を果たし、オートファゴソームのカーゴを選択的にリクルートするアダプタータンパク質としても機能します。TREM2変異をもつアルツハイマー病患者の組織ではLC3陽性ミクログリアの増加が見られ、TREM2依存的なオートファジーの阻害がアルツハイマー病の病因に寄与する可能性があります。
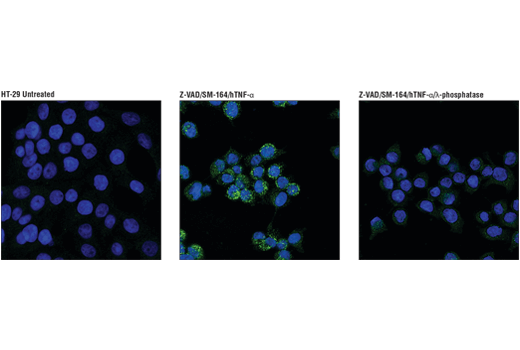
ヒトリン酸化RIP3 (Ser227) は、MLKL1をリン酸化してTNF誘導性ネクロトーシスを引き起こします。この形態のプログラムされた細胞死は、多発性硬化症と筋萎縮性側索硬化症で報告されています。