神経科学の基礎について学ぶ
神経科学とは?
神経科学は脳と脊髄、中枢神経、末梢神経を含む神経系の研究です。脳がどのように形成されて組織化され、どのように機能するのかという疑問を中心とした議論が最先端科学研究でも活発に行われています。また、慢性疼痛、精神疾患、神経発生疾患、神経変性疾患などの神経疾患の治療と予防は現代医学でも先端領域として注目されています。ここでは主に脳にフォーカスしますが、中枢神経と末梢神経で共通する部分もあり、下で説明した原理の多くは脊髄にも適用できます。
神経発生
神経発生では脳の発生を制御する分子や細胞イベントにフォーカスします。ヒトの場合、中枢神経系 (CNS、脳と脊髄) の発生は妊娠3週目 (GW3) に神経堤が生じて外胚葉から神経管が形成されることから始まります。神経管の癒合によって神経上皮が形成されます。神経上皮は多分化能をもつ幹細胞で構成される単一細胞層です。様々な段階的なシグナルによって神経管の背部、腹部、前部、後部に特有の神経上皮ニッチが形成されます。これらのユニークな神経上皮前駆細胞 (NEP) は神経管の領域化に寄与し、時間の経過とともに増殖、移動、分化して最終的に脳と脊髄の特有な構造を形成します。領域パターン形成シグナルに曝されることで、神経管の前後軸と背腹軸に沿ったNEPの位置によって特性が定義され、この特性はそれらの子孫細胞にも受け継がれます。
妊娠5週目 (GW5) までにニューロンの産出 (ニューロン新生) が始まり、これはGW8からGW25の間にピークに達し、妊娠中期には大部分が終了します。胚のニューロン新生は、脳脊髄液が循環する脳室に沿った特定の領域で起こります。NEPが急速かつ大規模に増殖するこの領域は胚帯と呼ばれます。神経発生の原則として、神経前駆細胞の多分化能は時間経過や細胞分裂の繰り返しによって徐々に制限されていきます。したがって、細胞の運命決定は個々の細胞の発生段階の後半でなされます。GW8までに数回の細胞分裂を経て、神経前駆細胞は有糸分裂後ニューロンに分化し始めます。これらの運命制限された有糸分裂後ニューロンは、産出された脳室近傍から離れて皮質板に移動します。皮質板は将来の大脳新皮質の一部となる一時的な構造です。ニューロンの移動はGW12からGW20にピークに達し、GW29までに完了します。したがって、新皮質の層状化 (異なる6層への細分化) は妊娠中の早い段階にコード化されます。ニューロンの移動が始まると、内側から外側に向かって層構造が形成されます。すなわち、表層 (軟膜に近い側) より深層 (脳室に近い側) の方が先に形成されます。
ニューロン新生と同様に、グリア新生 (CNS内の「マクロ」グリア細胞の産生) は、胚発生中に起こります。アストロサイトとオリゴデンドロサイトがNEPから産生されるグリア新生のピークはGW20からGW40で、ニューロン新生のピークが過ぎた後です。ミクログリアの産生と成熟はゆっくり時間をかけて起こります。最初のコロニー形成はGW9にみられますが、これはGW22を経て拡大し続けます。成熟したミクログリアはGW35にみられます。
ニューロン間のシナプス結合の形成も胚発生中に起こるプロセスの一つです。最も早いシナプスは脊髄でGW8前後、脳でGW9〜10にみられます。脳に皮質板が形成された後、皮質のシナプス形成は徐々に増加してGW28にピークに達します。死後脳を核磁気共鳴 (MRI) で神経解剖学的に解析した結果から、ニューロンはこの時点で原始的なネットワークに接続し、これが妊娠後期までの主要な繊維経路の形成を促進することが分かっています。したがって、一般に脳の神経回路マップの基本的な枠組みは、出生前期間の末期までに設定されます。しかし、シナプス結合は経験や環境変化に応じて、生涯を通じて動的に変化します。
新皮質の拡大、髄鞘の形成、シナプス形成は妊娠中に達成されますが、出生後も脳の成長は継続されます。実際に脳は成人までにサイズが4倍に増加します。6歳までに成人の90%まで増加し、思春期の間も増加を続けます。この年齢を超えて成人期まで成長を続ける特殊な皮質領域もあります。出生後の継続的なシナプスの再編成が神経可塑性の基本原理ですが、胚発生の間に構築された枠組みを基盤にして、出生後の神経回路や神経機能が形成されるのは明らかです。
ニューロンとグリア細胞の種類
上記のように、ニューロンとマクログリア (アストロサイトとオリゴデンドロサイト) は共通の前駆細胞集団から分化します。これに対してミクログリアはCNS外部でマクロファージから発生し、循環器系と脳室系を経て脳に移動します。
長い間、ニューロンがCNSの主役であり、グリア細胞はただの支持細胞であると考えられてきました。しかし、近年の多くの研究成果から、ニューロンとグリア細胞はともに脳機能の調節に重要な役割を果たし、それ故にどちらも神経疾患に深く関わることが分かってきました。脳の細胞は通常、その形態とマーカータンパク質の発現をもとに分類されます。以下に、これらの主要な細胞集団についてより詳細な説明をします。
ニューロン
ニューロンはCNSの特殊化した細胞で、電気化学的シグナルを処理する機能をもち、活動電位のを授受を行います。ニューロンは通常、神経細胞体 (soma) と呼ばれる細胞体、樹状突起と呼ばれる情報を受け取るための枝分かれした細胞突起、軸索と呼ばれるほかのニューロンに情報を伝えるための細長く伸びた細胞突起から成る複雑な形態をしています。軸索の長さはまちまちで、遠距離のニューロンどうしをつなぐため非常に長く伸びたものもあります。
ニューロンはさらに、発現する神経伝達物質、極性、形態、解剖学的な局在、情報を伝える方向に基づいて細分化することができます。
- 神経伝達のタイプ:ニューロンは、放出する神経伝達物質が標的ニューロンを脱分極させる (膜電位を正に変化させる) か、過分極させる (膜電位を負に変化させる) かによって、興奮性と抑制性に分類することができます。
- 極性:細胞体に対する軸索と樹状突起の向きによって、興奮性ニューロンを大きく4つのグループに分類することができます。
- 単極性:突起を1つのみ持つ (昆虫のみにみられる)
- 双極性:2つの原型的な伸張を持つ (1つの軸索と、最終的に樹状突起に分岐する1つの基底樹状突起)
- 多極性:1つの軸索と多数の樹状突起を持つ
- 偽単極性:軸索と樹状突起の両方の役割を果たす1つの伸長を持つ
- 形態:細胞体の形状と大きさ、突起の極性を基に、興奮性ニューロンをさらに分類することができます。
- 解剖学的な局在:ニューロンがCNS内に局在する位置によって、特定の特性が付加されるため、ニューロンを分類する際に考慮すべき点です。
- 情報の流れ:特化した突起によってニューロンには情報伝達の方向性が生じます。
- 求心性ニューロン:器官や特定の組織からCNSに情報を伝えるニューロン
- 遠心性ニューロン:CNSから器官や特定の組織に情報を伝えるニューロン
- 介在ニューロン:CNS内で別のニューロンに情報を伝えるニューロン
突き詰めると、これらの特性を組み合わせることでCNSのあらゆるニューロンを特徴付け、分類することができます。これによって特定のニューロンの機能と接続に関する具体的な情報を得ることができます。神経細胞体がみられるCNSの領域は「灰白質」と呼ばれ、軸索がみられるCNSの領域は「白質」と呼ばれます。白質の詳細については、「オリゴデンドロサイトとシュワン細胞」のセクションで説明します。
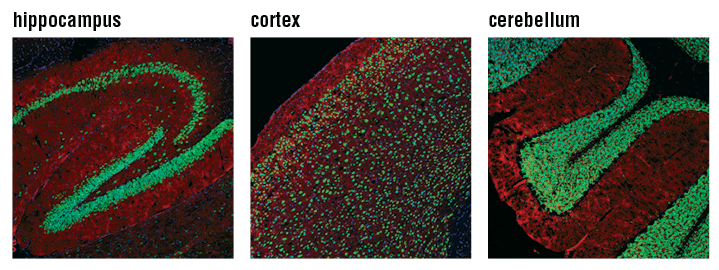
NeuN (D4G4O) XP® Rabbit mAb #24307 (緑) を用いてマウス海馬 (左)、大脳皮質 (中央)、小脳 (右) を染色し、共焦点蛍光顕微鏡で解析しました。アクチンフィラメントは、DyLight 554 Phalloidin #13054 (赤) で染色しました。DRAQ5 #4084 (蛍光DNA色素) は、青の疑似カラーで示しています。
ミクログリアとアストロサイト
アストロサイトとミクログリアはともに免疫関連細胞です。かつては脳における有害刺激への免疫応答のみに寄与すると考えられていましたが、アストロサイト、ミクログリアともニューロンの活性化とシナプス伝達の調節に新たな役割があることが分かってきました。
ミクログリアはCNSに常在する免疫細胞です。これらは骨髄細胞系列から発生し、胚発生初期に脳に侵入します。脳で急速に増殖して成熟し、白質と灰白質の両方に分布します。ミクログリアは発生中や成体のニューロン新生領域で、複雑な神経回路形成の制御に寄与しています。これらは不要なニューロン、シナプス、樹状突起を剪断して除去します。また、これらはある種の神経伝達物質受容体をもち、ニューロンからの神経伝達物質の放出に応答してシナプスの可塑性を補助することができます。さらに、ニューロンから過剰量の興奮性神経伝達物質が放出された場合に興奮毒性を抑える機能もあります。
ミクログリアは病態、特にタンパク質の凝集がみられるアルツハイマー病 (AD)、パーキンソン病 (PD)、筋萎縮性側索硬化症 (ALS) などの神経変性疾患においても重要な役割があります。健常状態ではミクログリアは休止状態にありますが、脳への感染や急性外傷によって活性化されて炎症促進分子を放出し、炎症反応を開始します。ある場合には、不要な細胞片をミクログリアが貪食して除去することもあります。これは急性応答で、通常は時間の経過とともに解決されます。しかし、病態においては凝集したタンパク質やその他の長期にわたる有害刺激に応答した慢性炎症によって、グリオーシスと呼ばれる慢性的な炎症促進性の反応を引き起こします。これはニューロン、アストロサイト、オリゴデンドロサイトに非常に有害です。すなわち、ミクログリアは急性の有害なイベントから脳を保護する機能を持ちますが、疾患状態によってミクログリアが長期にわたって活性化されると疾患の進行に寄与するようになります。
ミクログリアとは異なり、アストロサイトはCNSで産生されます。これらは脳血液関門を形成する血管内皮細胞を支持する機能があり、有害な刺激に応答して反応するため、脳の免疫に寄与すると考えられています。また、アストロサイトはCNSの損傷後の瘢痕形成や修復に寄与しています。一方、ニューロンとアストロサイトの強い相互作用によってCNSにおけるアストロサイトの機能の多様性が強化されます。例えば、アストロサイトは神経機能に影響を及ぼすある種のイオンの細胞外濃度を緩衝し、ある種の神経伝達物質に応答して自身が神経伝達物質 (グリオトランスミッター) を放出することもできます。また、ニューロンとアストロサイトには代謝的に密接なつながりがあります。アストロサイトはニューロンに栄養素のサポートを行うだけでなく、重要な中間体を放出して神経伝達物質の生合成を補助します。ミクログリアと同様に、アストロサイトはシナプスと形成と維持にも寄与します。さらにミクログリアと同様に、慢性的な疾患状態がアストロサイトの長期にわたって活性化し、アストログリオーシスを引き起こします。そのため、ADやハンチントン病 (HD) など多くの神経変性疾患で、アストロサイトに起因する障害がみられます。
アストロサイトとミクログリアのクロストークは、健常状態と疾患状態の両方でそれぞれの機能の変調、悪化、消滅の原因となり、これが脳全体の機能に影響を及ぼします。
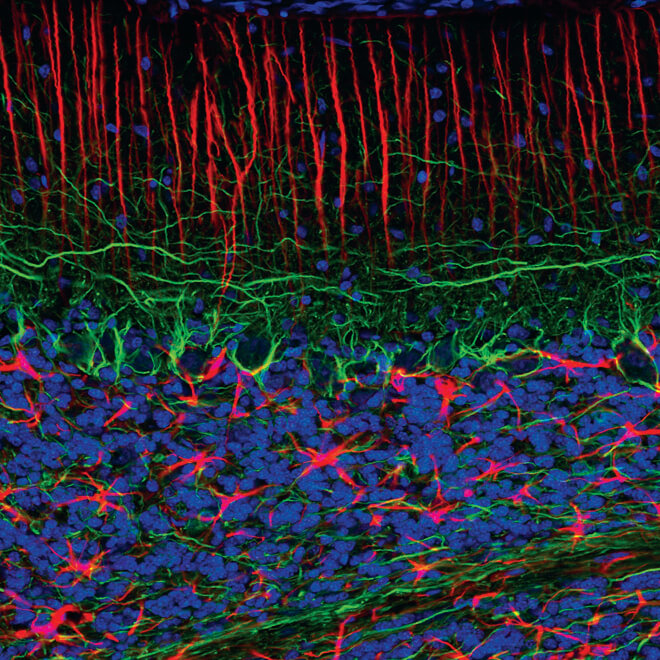
GFAP (GA5) Mouse mAb (Alexa Fluor® 555 Conjugate) #3656 (赤) およびNeurofilament-L (C28E10) Rabbit mAb #2837 (緑) を用いて正常ラット小脳を染色し、共焦点蛍光顕微鏡で解析しました。DRAQ5 #4084 (蛍光DNA色素) は、青の疑似カラーで示しています。
オリゴデンドロサイトとシュワン細胞
オリゴデンドロサイト (OL) はミエリンを産生するCNSの細胞です。原則としてオリゴデンドロサイトの新生は常にニューロンの新生に引き続いて起こり、通常は脳や脊髄のニューロンと同じ領域で起こります。成熟したOLはミエリンと呼ばれる脂質に富む膜を産生し、これが軸索を絶縁してニューロンの電気信号の伝達速度を高めます。髄鞘 (ミエリン) 形成のプロセスは脊髄でGW12、脳でGW14に始まり、出生後は1年のみ強固に行われ、30年まで続きます。シュワン細胞は末梢神経系に存在するOLと同等の細胞です。
髄鞘の形成は動的なプロセスで、神経伝達を増強するようによく調整されています。オリゴデンドロサイト前駆細胞の再生プールは脳内に残り、生涯を通じて必要に応じてOLが産生されます。オリゴデンドロサイトの新生は外傷によってミエリンが損失した場合や、神経回路の変化で髄鞘の再編成が必要になった場合に引き起こされます。しかし、このような前駆細胞が存在するにも関わらず、加齢に伴う髄鞘形成の低下が認知症の発症や認知機能の低下に関与しています。また、ADや多発性硬化症 (MS) などの神経変性疾患でミエリンの損失がみられます。
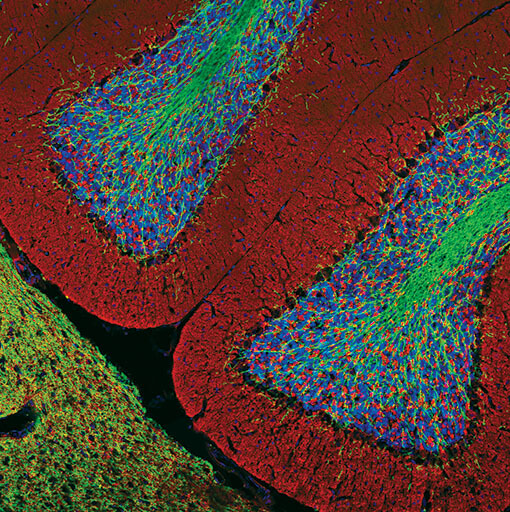
Myelin Basic Protein (D8X4Q) XP® Rabbit mAb #78896 (緑) およびSynaptophysin (7H12) Mouse mAb (IF Formulated) #9020 (赤) を用いてラット脳を染色し、共焦点蛍光顕微鏡で解析しました。DRAQ5 #4084 (蛍光DNA色素) は、青の疑似カラーで示しています。
神経系の機能
ニューロンとグリアの相互作用は神経系の機能を調節します。以下で、ニューロンが外部から情報を受け取り、ニューロン内部で電気信号を伝播する細胞内イベントについて説明します。これらはともに、CNS機能を調節しています。
シナプス活性
上記のように、ニューロンは電気化学的シグナルの処理に特化した細胞です。ニューロンはシグナルの入力と出力を担う突起 (それぞれ樹状突起と軸索) をもっています。シグナルを発するニューロンをシナプス前細胞、シグナルを受け取るニューロンをシナプス後細胞、この2つの間の細胞外空間をシナプスと呼びます。
シナプス前細胞のリガンドと電位依存性イオンチャネルによって、ニューロンの細胞内電位 (膜電位とも呼ばれる) を変化させるイオンの流入を起こすことができます。ニューロンの静止膜電位は、通常–50から-70 mVです。陽イオンが急速に細胞に流入することでシナプス前細胞の脱分極が起こり、これがある閾値に達するとニューロンは活動電位を発生させます。これは電位の変化に応答した「全か無か」の反応で、活動電位はシナプス前終末に到達するまで軸索全体を伝播します。シナプス前終末には神経伝達物質を内包した小胞が待機しており、カルシウム依存的なシナプス前膜との膜融合の準備を整えています。活動電位がシナプス前終末に到達すると、そこに存在する電位依存性カルシウムチャネルによってカルシウムの流入が起こり、神経伝達物質を内包したシナプス小胞が膜に結合してこれらの分子を細胞外に放出します。神経伝達物質はシナプスを横断し、シナプス後細胞の樹状突起の小区画 (スパイン) にある受容体に結合します。
神経伝達物質が放出され、それが受容体に結合すると、シナプス後細胞に陰性イオンまたは陽性イオンが流入し、それぞれ抑制性または興奮性に作用します。陽性イオンがシナプス後細胞を脱分極させることで活動電位が発生します。しかし、陰性イオンがシナプス後細胞を過分極させた場合や脱分極が起こらなかった場合には活動電位は発生せず、電子信号の伝播は起こりません。シナプス前細胞では、活動電位が一旦通過すると、細胞内環境を平常化するイオンチャネルやATP依存性トランスポーターの作用で細胞の再分極が起こります。不応期と呼ばれる短時間の過分極ステージでは活動電位は発生しません。このステージを過ぎると細胞は再び脱分極できるようになります。シナプス前細胞の急速な活性化はシナプス後細胞の受容体プールに影響を及ぼし、これが相互作用の再編成につながります。これがシナプス可塑性の一形態です。その他の形態にはシナプスの剪定やグリアによる調節があります。
概日リズム
概日リズムは、様々な生物学的機能に24時間の周期性を付与する生物学的プロセスです。概日行動の最も顕著な例は睡眠と覚醒の周期ですこの周期は脳で処理される光信号に同調します。脳では、視床下部に存在するニューロンの一部が睡眠と覚醒の周期のタイミングを制御する中心的なペースメーカーとして機能します。これらは代謝や記憶固定などの他の反応の重要な間接的制御因子となります。したがって、脳はCNSの機能をサポートする形で概日リズムの種のような役割を担っています。
感覚系と運動系
感覚系と運動系は、末梢神経の活動に大きく依存しています。皮膚の感覚機能の刺激は脊髄や脳でシナプスを形成する神経のネットワークを介して伝達されます。身体のそれぞれの特定の領域の感覚や運動機能に対応する脳の領域は、「ホムンクルス」と呼ばれるトポグラフィックマップにまとめられています。末梢から脳への神経のルートは制限されているため、感覚機能や運動機能の障害がみられる場合、精密な解剖学的マップを用いて病変部位を特定することができます。
内分泌系
内分泌系と神経系には密接な関わりがあります。ホルモンは摂食と代謝、神経伝達物質の生合成と放出、血管機能と血流、さらには出産など、脳に直接的または間接的に影響を及ぼす多くのプロセスを調節するだけでなく、脳機能の多くの側面を調節します。ホルモンは特定の神経回路に影響を与え、反応をさらに強化したり、その消滅に寄与したりします。さらに、エストロゲンによる性差は脳の発達の顕著な要素であり、女性の閉経によるエストロゲンレベルの変化が、加齢に伴う脳機能の変化に関与する可能性があります。内分泌系と神経系の相互接続は全体的な機能に影響を及ぼすもう一つの調節レベルです。
神経系の障害
神経系の障害は複数のカテゴリーにまたがります。下にこれらを簡単に説明します。
神経変性
「神経変性」という用語は通常、CNSにおけるニューロンやグリアの欠落をもたらす障害のことを指します。神経変性には、加齢性疾患に関連するもの (AD、PD、認知症)、神経系に対する自己免疫反応に関連するもの (MS)、CNS細胞の健康に影響を与える遺伝子変異に関連するもの (HD、早期発症AD / PD、ALS)、脳への力学的な傷害が関連するもの (慢性外傷性脳炎) があります。これらの疾患のいくつかについて下で説明します。
5.1a アルツハイマー型 (AD)
アルツハイマー病 (AD) は、世界で約5千万人もの人が罹患している疾患で、この数は今後10年間で徐々に上昇し、世界的な公衆衛生を圧迫することが予測されています。
ADの特徴に、細胞の内外に老人斑や神経原線維変化として知られるタンパク質凝集体を形成することが挙げられます。これらの病原タンパク質に沿って複数の脳領域で広範なニューロンの欠落が起こり、徐々に認知機能が低下します。上記のように、ADにはニューロンだけではなくグリアも深く関与しています。しかし、これらがADの一次的なエフェクターであるのか、二次的な関連事象であるのかははっきりしていません。
一般にADは加齢に伴う疾患であると考えられていますが、ある種の遺伝子変異がADの早期発症に関与しています。両方のタイプのADの病態形成に関わる主要な分子を同定し、解析を行うためにこれらの遺伝子が研究されてきました。これらの遺伝子や遺伝子産物 (タンパク質) を標的とした医療と、有害なタンパク質凝集体に対するワクチンを開発することが、ADと戦うために広く利用されている2大戦略です。今日までADの治療法は見つかっていません。
5.1b パーキンソン病 (PD)
ADと同様、パーキンソン病 (PD) は加齢に伴う疾患でもあり、遺伝的要因も持つ疾患です。タンパク質の凝集もPDの特徴ですが、これらの凝集体の原因はADより複雑です。これは家族性または若年性PDに関連する遺伝子がADよりはるかに多いためで、PDの治療法の開発をより複雑化させています。PDでは始めに運動機能の障害がみられますが、進行性の神経変性によって認知機能の低下がみられるようになります。
5.1c 多発性硬化症 (MS)
多発性硬化症 (MS) では、免疫系が脳と脊髄の神経軸索を囲む髄鞘を攻撃し、神経伝達の低下と軸索そのものの劣化を引き起こします。MSは運動能力の変化をもたらし、視覚、痛覚処理、発話、気分により広範な影響をもつ可能性があります。MSの正確な病因は不明ですが、女性の発症率が2倍高く、人種や環境要因が危険因子となります。
5.1d 筋萎縮性側索硬化症 (ALS)
筋萎縮性側索硬化症 (ALS) は筋肉を刺激する脳や脊髄のニューロンを特異的に侵します。これらは運動ニューロンです。運動ニューロンの進行性の変性と欠落がみられ、CNSが筋肉の動きを制御できなくなります。この結果、発話、運動、摂食に障害が起こり、最終的に呼吸ができなくなります。ALSの症例の90〜95%が孤発性で、5〜10%が家族性です。ALSの特定の原因は不明ですが、遺伝子変異、神経伝達の変化、タンパク質の処理が発症に関与しています。
神経発達障害
神経変性疾患とは異なり、神経発達障害はCNSの発達中に起こります。これらには遺伝的要因に基づくもの (自閉症、ダウン症候群、脆弱X症候群)、環境要因に誘発されるもの (胎児性アルコール症候群)、あるいは特発性のもの (自閉症) があります。
5.2a 自閉症
自閉症は、妊娠期間中または思春期のCNS発達の変化に起因する神経発達障害です。自閉症は遺伝子変異、環境要因、ある種の感染、出生児の低酸素症によって起こります。自閉症は非常に複雑な疾患で、症状にも個人差があります。自閉症の一般的な特徴は、社会性やコミュニケーション能力の障害と繰り返し行動です。これらの一般的な特徴は軽度から重度まで様々で、不安、多動、感覚処理の障害、痙攣、睡眠障害、胃腸疾患、気分変動などの症状を伴うことがあります。
5.2b ダウン症候群 (DS)
ダウン症候群 (DS) は常染色体の異数性による疾患としてよく知られています。米国では約400,000 人が罹患しており、毎年5,300人のダウン症の新生児が誕生しています。DSは21番染色体トリソミーとしても知られ、純粋に遺伝的要因に基づいています。DS罹患者にはCNSの発達や成長の異常がみられ、認知機能の変化がみられるため、神経発達障害とみなされます。DS罹患者にはニューロンやグリアの増殖や成熟速度に遅延がみられ、生涯にわたって神経伝達や機能に広範な異常がみられます。さらに21番染色体上の1つの特定のAD関連遺伝子が3倍体化するため、DS罹患者はADも発症しやすくなります。
精神障害
精神障害は通常、神経伝達物質の不均衡によって発生します。統合失調症がその1例です。統合失調症は遺伝的要因または環境要因による慢性的な精神障害です。神経伝達の異常がこの障害の特徴で、これは神経伝達物質のレベルの異常や妊娠期の脳の発生の異常に起因すると考えられています。また、思春期に起こる内分泌系の変化が統合失調症の原因となる可能性がありますが、正確な発症の原因は分かっていません。統合失調症の根本的な原因が明らかにされていないため、治療法は対症療法に限られ、抗精神病薬から心理療法にまで及びます。
疼痛性障害
疼痛障害は日常生活が妨げられるほどの慢性的な疼痛によって特徴づけられます。一部の疼痛障害には心理的な要因が関与すると考えられていますが、末梢神経 (すなわち末梢神経障害) やCNSの健康状態に起因する場合もあります。例えば、抹消神経障害は外傷、遺伝的要因、有害物質への暴露、糖尿病などの代謝疾患によって引き起こされることがあります。線維筋痛症はもう1つの疼痛障害で、繰り返しの神経刺激を引き起こす筋骨格痛が特徴です。これによって神経可塑性が誘導され、脳による疼痛刺激の神経伝達と処理が変化します。
神経科学の研究法
神経科学は通常、モデルシステム、ヒト死後組織、患者のイメージング技術を利用して研究されています。モデルシステムと特定の組織ベースの技術について下で説明します。
モデルシステム
最も古典的な神経科学のモデルシステムはイカの巨大軸索です。このシステムは軸索を容易に単離することができ、顕微鏡を用いずに可視化できるため有用でした。古典的な活動電位の伝播や神経伝達物質の放出の研究は、このイカの巨大軸索を用いて行われました。より近代的には、ショウジョウバエから線虫、ゼブラフィッシュ、マウス、ラット、フェレット、ヒト以外の前霊長類までがモデル生物として利用されています。ショウジョウバエ、線虫、げっ歯類のモデルシステムでは、遺伝子操作を用いて神経回路の重要な側面の解析や機能に不可欠なタンパク質の単離を行うことができます。さらに、特定の疾患の原因となる変異をこれらの生物に導入することができ、CNSの機能を生理学、分子生物学、解剖学、性状など様々な側面を研究することができます。また、これらの生物や、ヒトの健常組織、疾患組織に由来する細胞をモデルとして用いることもできます。
技術
神経科学の技術には、基礎的な細胞、分子技術から電気生理学的試験、抗体技術を利用してin situで可視化するイメージングベースの技術まであります。
特にin situ組織染色は柔軟性が高く堅実で情報量の多い手法で、解析対象のタンパク質を識別して細胞内局在を特定し、これらのタンパク質の相互作用を可視化するのに利用できます。個々のニューロンやグリアの細胞集団を軸索、樹状突起、受容体、内包する神経伝達物質に基づいて特性解析することができます。さらに、病態において変化したタンパク質を選択的に追跡し特性解析することもできます。Cell Signaling Technologyは、このようなin situ検出や、その他の手法で解析対象を識別する神経科学ツールの豊富なレパートリーを保有しています。