細胞死の概要
細胞死のメカニズムと種類
細胞は、その状況やトリガーとなる刺激に応答し、様々な種類の細胞死を起こします。
細胞死の種類
細胞死のメカニズムとしては、以下のものがあります。
- アポトーシス :発達や発生過程において、また有害な環境刺激に応答して起こる、プログラムされた細胞死です。
- ネクローシス:ネクロプトーシスやパイロプトーシスのような、受動的あるいは能動的な制御されたプロセスです。
様々なアッセイを利用して、細胞死のメカニズムを特定したり、細胞集団における特定の細胞死メカニズムを除外したりできます。
アポトーシス
アポトーシスは、厳密に制御されているプログラムされた細胞死であり、多細胞生物の発生、発達、および細胞ストレスに応答して起こります。アポトーシスは、カスパーゼと呼ばれるタンパク質分解酵素ファミリーによって仲介されます。アポトーシス促進タンパク質や抗アポトーシスタンパク質など、その他のタンパク質も重要な役割を担います。
アポトーシスの制御異常は、自己免疫疾患、神経変性疾患、がんなどにみられます。
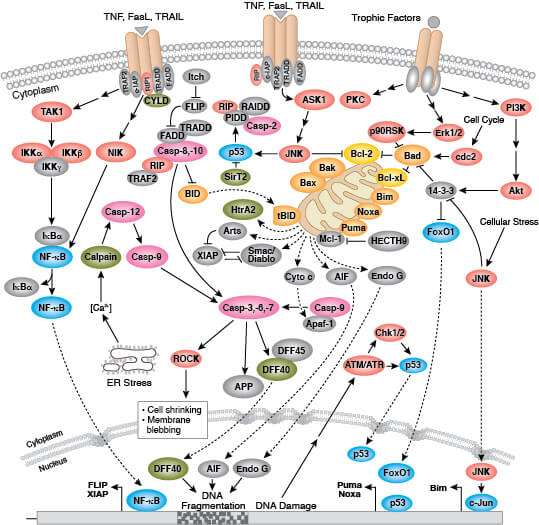
アポトーシスは、カスパーゼやその他のタンパク質によって仲介される、プログラムされた細胞死です。
アポトーシス制御:インタラクティブパスウェイ図はこちら >>アポトーシスの測定方法
アポトーシス細胞は、表現型の変化や特定のタンパク質の活性によって生細胞とは区別できます。細胞集団におけるアポトーシスレベルの解析および測定には、いくつかの異なる手法があります。以下のアッセイをご覧ください:
アッセイ
測定対象
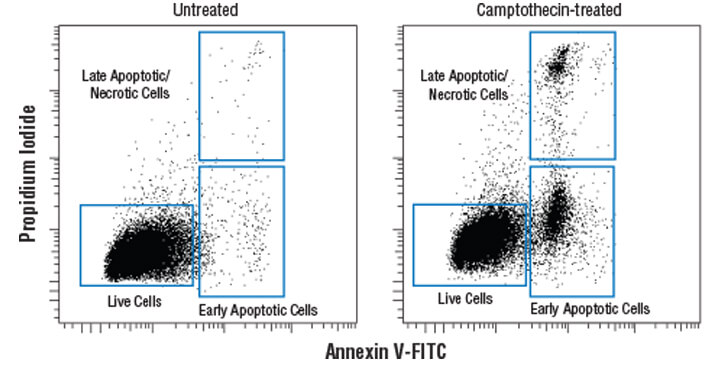
アポトーシスの初期に起こる脂質二重層の変化を検出します
アッセイ
TUNELキット
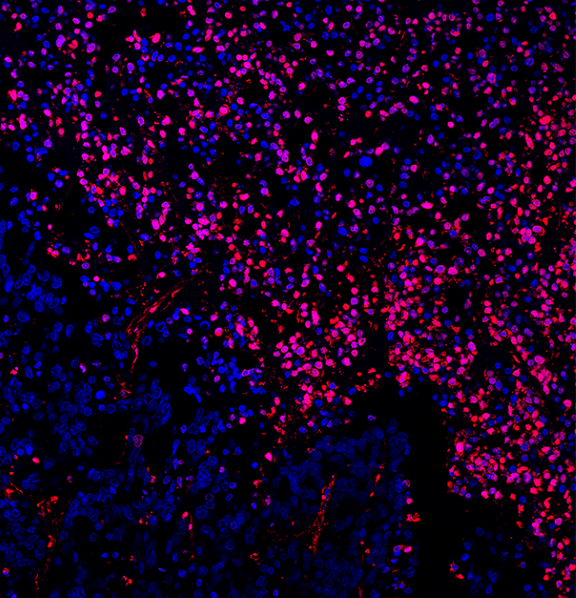
アポトーシスの特徴であるDNAの断片化を検出します
測定対象
アッセイ
カスパーゼの切断
測定対象
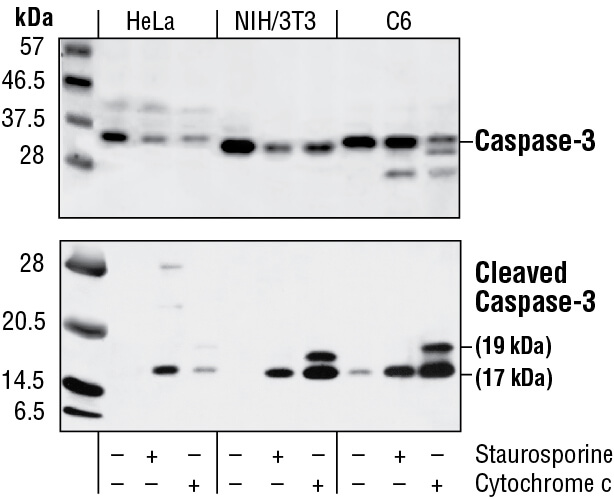
Caspase-3の切断、カスパーゼ活性アッセイ、その他のカスパーゼやPARPの切断は、アポトーシスの測定によく使用されます
アッセイ
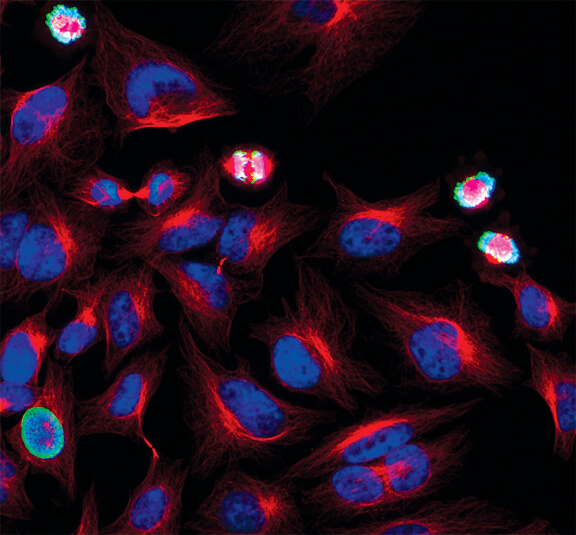
クロマチンの凝縮
測定対象
DAPIやHoechst 33342などの核染色色素で染色した後、クロマチンが凝縮したアポトーシス細胞を検出します
アッセイ
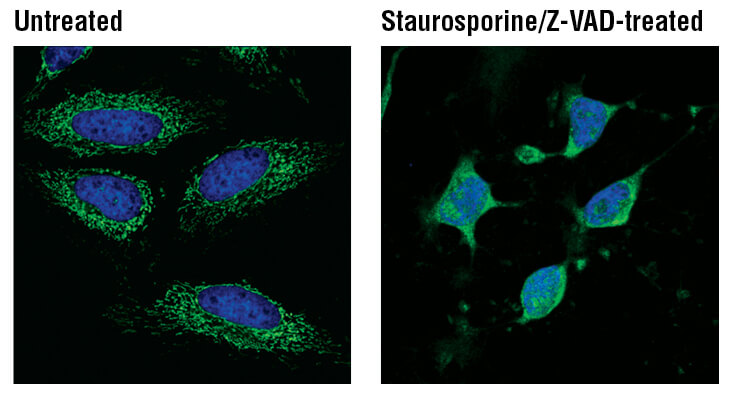
シトクロムcの放出
測定対象
ミトコンドリアから細胞質へのシトクロムcの放出は、アポトーシス細胞の特徴の1つです
アッセイ
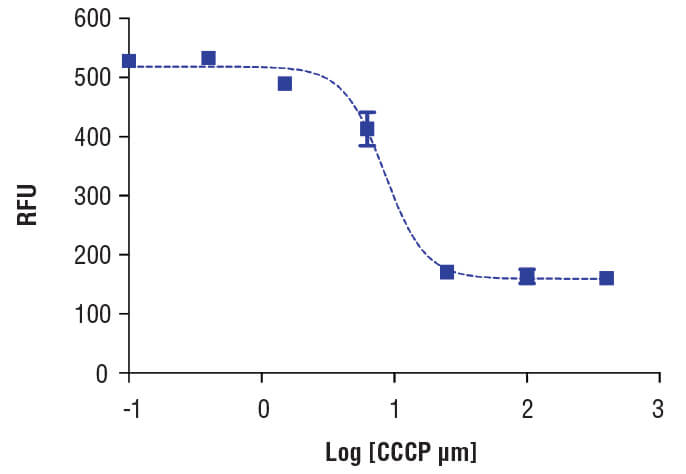
測定対象
脱分極とそれに続くミトコンドリア膜電位の低下は、アポトーシス細胞の特徴の1つです
ネクローシス
ネクローシス (壊死) は、急性傷害や感染症に続いて受動的に起こるプログラムされていない細胞死であり、アポトーシスが阻害された場合に起こります。細胞の腫脹や溶解を特徴とします。壊死した細胞は細胞の内容物を周囲の環境に放出しますが、これにより炎症応答が活性化され、食細胞が動員されて死細胞が除去されます。しかし、制御されていない場合、壊死は壊疽などの深刻な組織損傷を引き起こす可能性があります。
ネクローシスは、受動的でありプログラムされていない細胞死であると考えられてきましたが、近年の研究により、異なるタイプの制御されたネクロプトーシス経路の存在が明らかになりました。
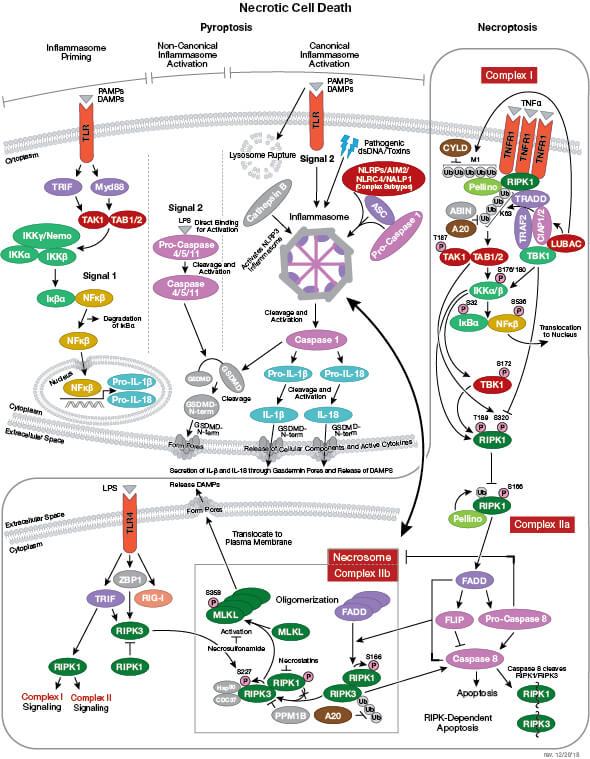
制御されたネクローシス
ネクローシスに加え、その他の溶解性細胞死のメカニズムとして、以下のものがあります。
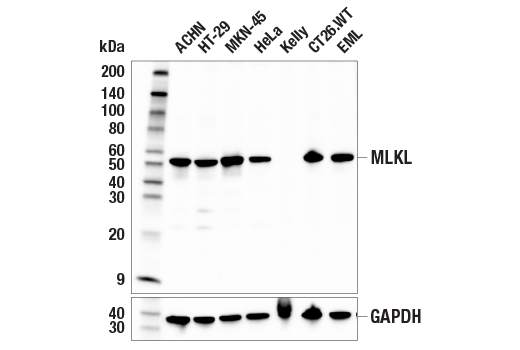
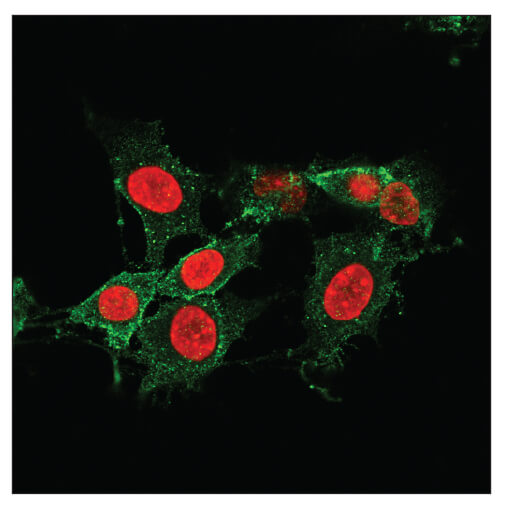
- ネクロプトーシス:プログラムされている制御された壊死の一形態であり、RIP3とMLKLを必要とし、虚血性傷害やウイルス感染だけでなく、炎症促進性シグナル伝達によっても活性化されます。
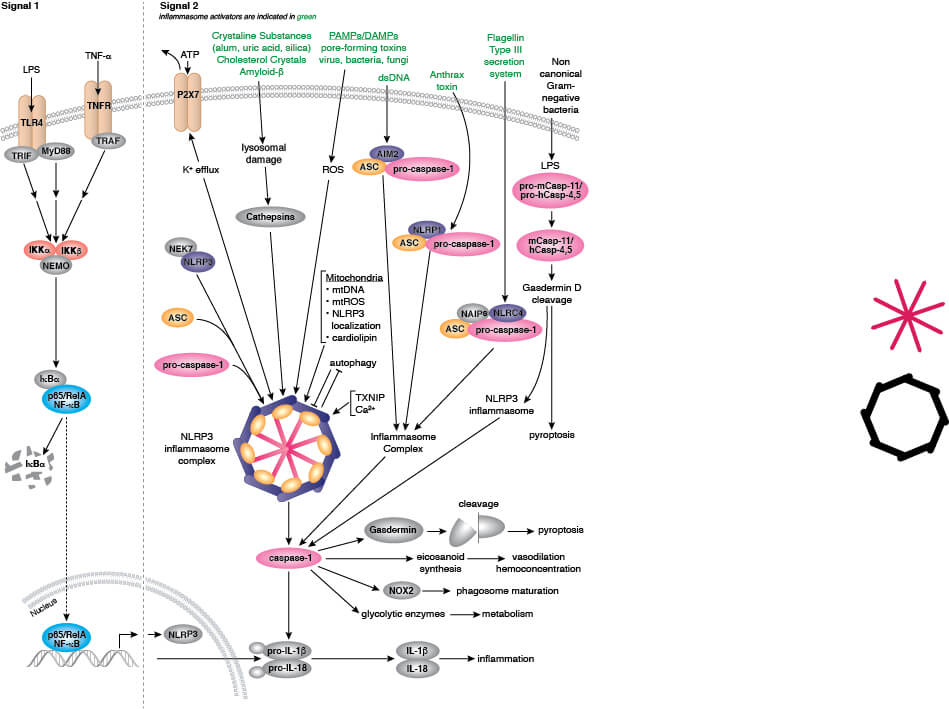
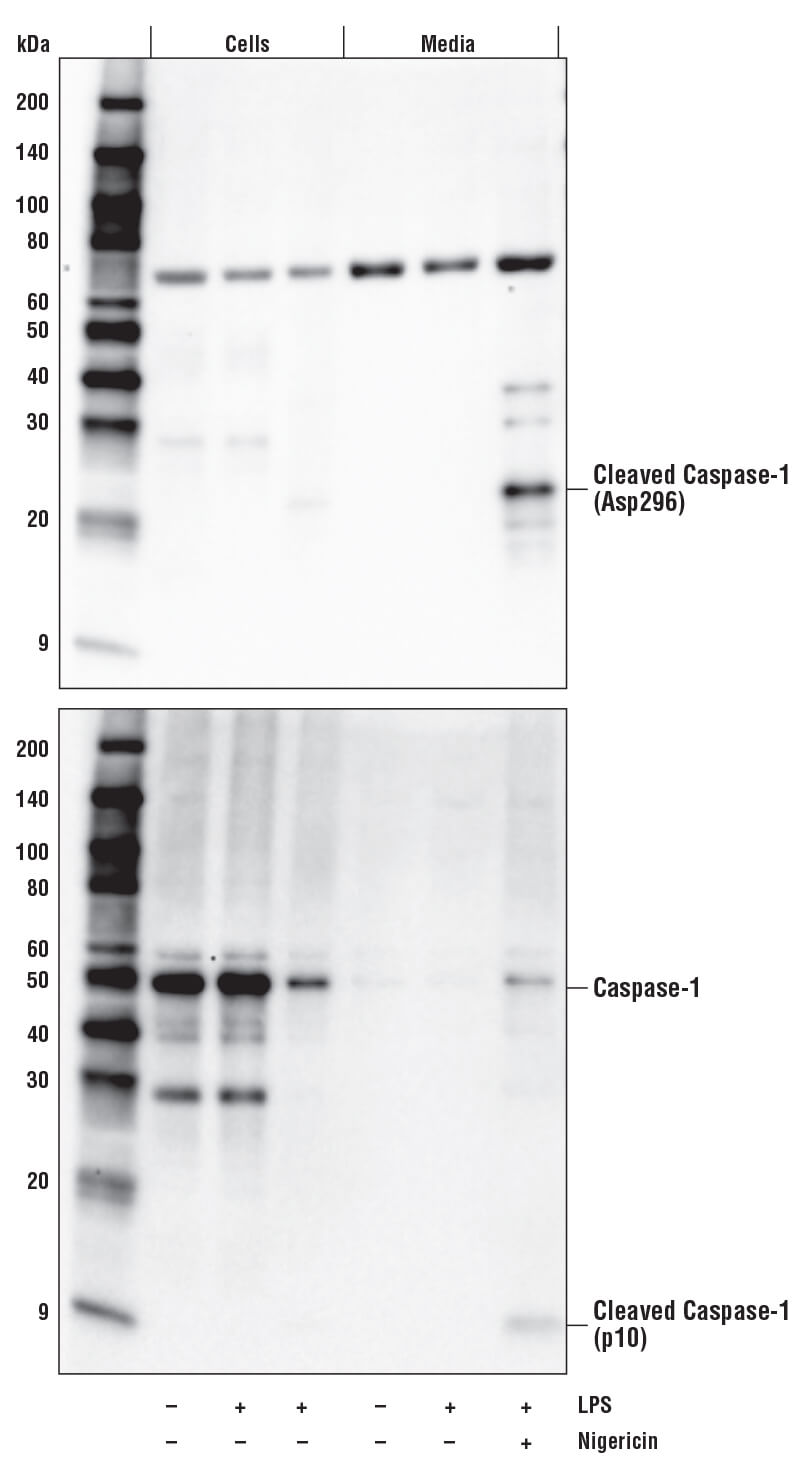
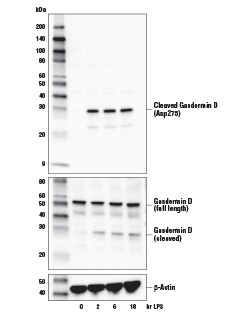
- パイロトーシス:プログラムされた溶解性細胞死の一形態であり、通常は、微生物やウイルス感染に対する応答として免疫細胞で発生し、Caspase-1とGasdermin-Dを必要とします。
ネクロプトーシスの測定方法:
ネクロプトーシスのマーカー
ネクロプトーシスマーカーの説明
炎症や細胞死を調節するSer/Thrキナーゼ
ネクロプトーシスのマーカー
ネクロプトーシスマーカーの説明
ネクロプトーシスに必要なSer/Thrキナーゼ
ネクロプトーシスのマーカー
ネクロプトーシスマーカーの説明
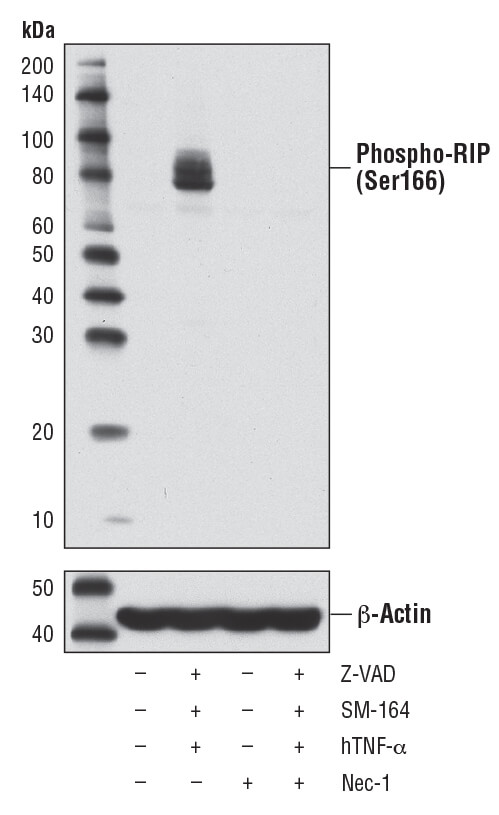
活性化したRIPはRIP3と連携し、ネクロプトーシスを誘発します
ネクロプトーシスのマーカー
ネクロプトーシスマーカーの説明
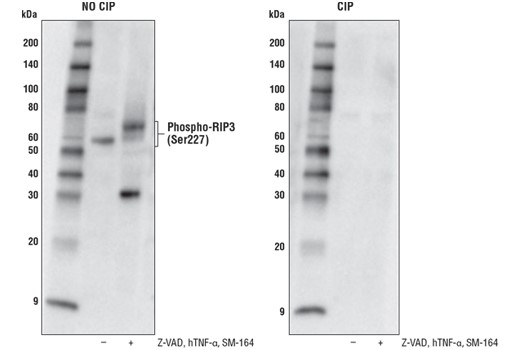
RIP3の活性化が、MLKLのリン酸化を誘導します
ネクロプトーシスのマーカー
ネクロプトーシスマーカーの説明
RIP3下流のタンパク質標的
ネクロプトーシスのマーカー
ネクロプトーシスマーカーの説明
MLKLのリン酸化は、ネクロプトーシス細胞のマーカーであり、細胞膜に小孔を形成します
ネクローシスの評価方法:
ネクローシスのマーカー
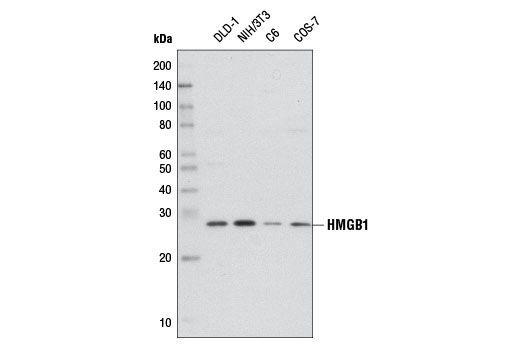
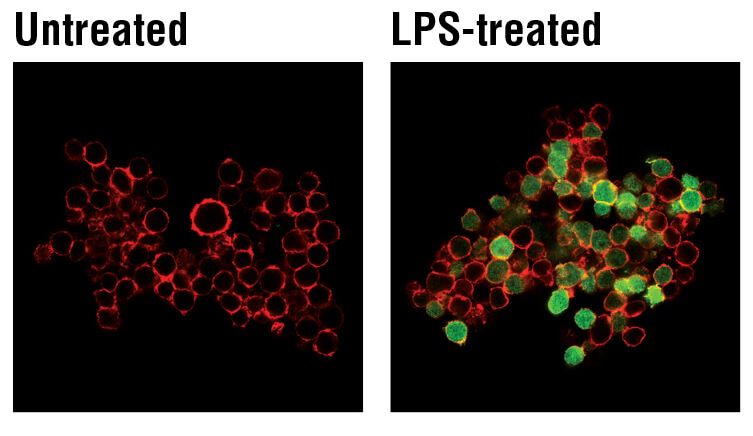
HMGB1 (High mobility group protein B1)
ネクローシスマーカーの説明
アポトーシス性ではなく壊死性の細胞死の際に細胞外環境に放出される核タンパク質
ネクローシスのマーカー
ネクローシスマーカーの説明
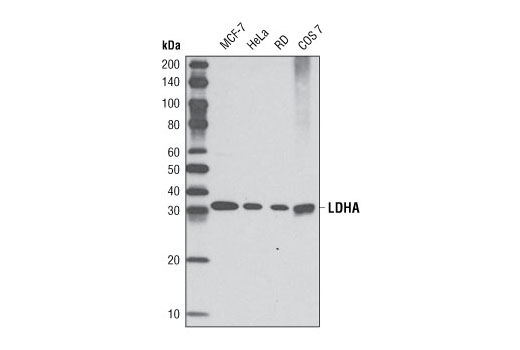
壊死性の細胞死の際に細胞外空間に放出される細胞質酵素
ネクローシスのマーカー
ネクローシスマーカーの説明
壊死の際に放出される炎症促進性サイトカイン